张 燕 ,王东云,王子龙 ,庞留勇 ,赵 中
(1. 黄淮学院 a. 化学与制药工程学院; b. 智能制造学院;
c. 数学与统计学院,河南 驻马店 463000;
2. 西交利物浦大学 理学院, 江苏 苏州 215000)
静脉注射具有生物利用率高、起效快和吸收迅速等优点,但长期静脉注射容易造成血管局部循环障碍,并导致组织缺氧,产生水肿和静脉炎等副作用。口服给药方式简便、安全,且价格比较低廉,但口服给药具有起效慢、生物利用率低等缺点。临床上为了发挥两种给药方式的优点,医疗工作者已经进行了口服联合静脉注射给药方式临床效果的研究。刘哲[1]研究了胺碘酮静脉注射联合口服用药治疗恶性心律失常的临床效果,结果表明:口服给药和静脉注射两种不同的给药方式在治疗恶性心律失常时,其临床疗效无明显差异,但静脉注射联合口服用药能够减少并发症的发生,降低疾病的复发率。杨汉杰[2]研究了静脉注射联合口服胺碘酮转复阵发性心房纤颤的疗效,结果发现:静脉注射联合口服小剂量胺碘酮胺碘酮可明显提高阵发性心房纤颤转复率,且具有较高的安全性。赵欢欢[3]研究了高龄胃肠道恶性肿瘤患者口服联合静脉注射化疗药物对不良反应发生率的影响,结果表明:口服联合静脉注射化疗药物,可以在治疗高龄胃肠道恶性肿瘤患者时起到降低不良反应发生率,提高治疗效果的作用。
目前已经有许多学者进行了给药方案设计的研究,周吉欽等[4]综述了万古霉素在不同人群中的药代/药效学(PK/PD),为万古霉素临床给药方案的优化指明了方向。李贺等[5]基于PK/PD理论,应用蒙特卡洛模拟方法,评价及优化了不同病原菌感染时帕珠沙星的给药方案,为帕珠沙星临床最佳给药方案的制定提供依据。
COOK等[6]基于早期临床实验评估模型和剂量递增策略,确定了药物的最优剂量和毒性评估。
YU等[7]采用蒙特卡罗模拟法研究了双氯西林口服给药方案 的设计问题,并给出了可用于临床的具体给药剂量方案。
然而,对于联合给药方案设计的研究文献较为少见,苏银法等[8]给出了静脉滴注和口服联合用药的Excel给药方案设计方法,但没有给出具体的理论分析。
本文利用脉冲微分方程,建立静脉注射联合口服给药方式的一房室药代动力学模型,给出静脉注射联合口服给药方案的理论分析,并借助计算机技术给出给药方案设计的具体方法,确保患者的血药浓度处于用药安全的治疗窗口之内。进一步地,通过具体的算例验证该方法的可行性和合理性。
为了便于讨论,静脉注射联合口服给药方式为:同时静脉注射剂量为d1的药物和口服剂量为d2的药物,经过时间间隔τ后,再次同时静脉注射剂量为d1的药物和口服剂量为d2的药物,依次进行,此联合给药方式和文献[2]的给药方式是一致的。
以时间间隔τ把整个给药过程分成若干个小区间[0,τ],(τ,2τ],…,(nτ,(n+1)τ],…,这里n为非负整数,则多个治疗周期的静脉注射联合口服给药方式的一房室模型如下:
(1)
其中:x=x(t)表示t时刻吸收位的药量,y=y(t)表示t时刻体液内的药量,k0表示药物的吸收率,k1表示药物的代谢率,f为口服药物的生物利用率。
系统(1)可以看成吸收位和体液两个药代系统的耦合。其中吸收位药量变化可以描述为:
(2)
体液药量的变化可以描述为:
(3)
先考虑吸收位药量的变化情况。在区间t∈(nτ,(n+1)τ]上求解式(2)可得
x(t)=x(nτ+)e-k0(t-nτ),
则有
x((n+1)τ)=x(nτ+)e-k0τ,
进而
x((n+1)τ+)=x(nτ+)e-k0τ+fd2。
(4)
由于e-k0τ<1,则易知式(4)存在一个稳定的不动点为
也即是系统(2)存在一个稳定的周期解。进而可知,稳态的情况下吸收位的药量将呈现周期性变化,变化规律为
x*(t)=x*e-k0(t-nτ),t∈(nτ,(n+1)τ],
n=0,1,…。
下面讨论在吸收位处于稳态的情况下,体液药量的变化情况。系统(3)的第一个方程可以变为
在区间t∈(nτ,(n+1)τ]上求解上式可得
y(nτ)e-k1(t-nτ),
进而有
则有
y(nτ+)e-k1τ+d1。
(5)
由e-k1τ<1,易知式(5)存在一个稳定的不动点
进而系统(3)存在一个稳定的周期解
(6)
这表明,体液药量也将呈现周期性变化。进一步地,还可以得到一个给药时间间隔的平均稳态药量水平为
当d2=0时(也即是单独的静脉注射的情况),可得
当d2≠0时,令dy*(t)/dt=0,可得药量的达峰时间为
此时对应的最大药量为
(7)
而稳态的最小药量为
(8)
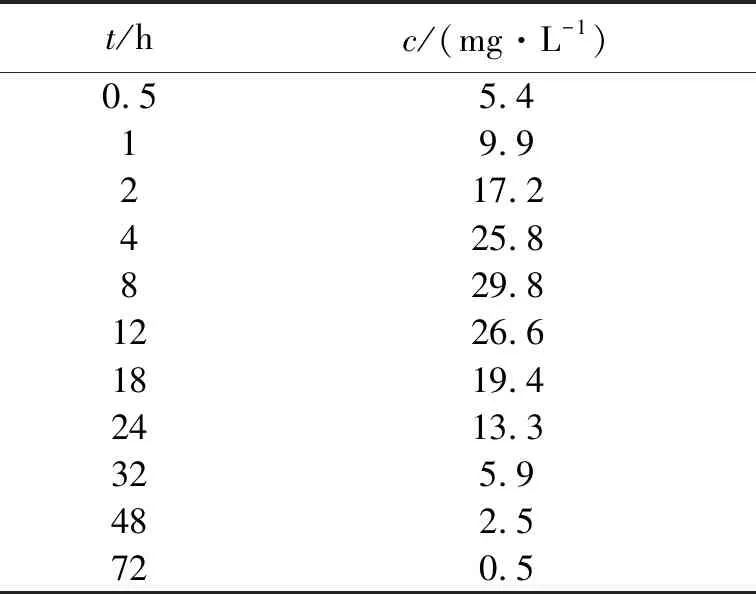
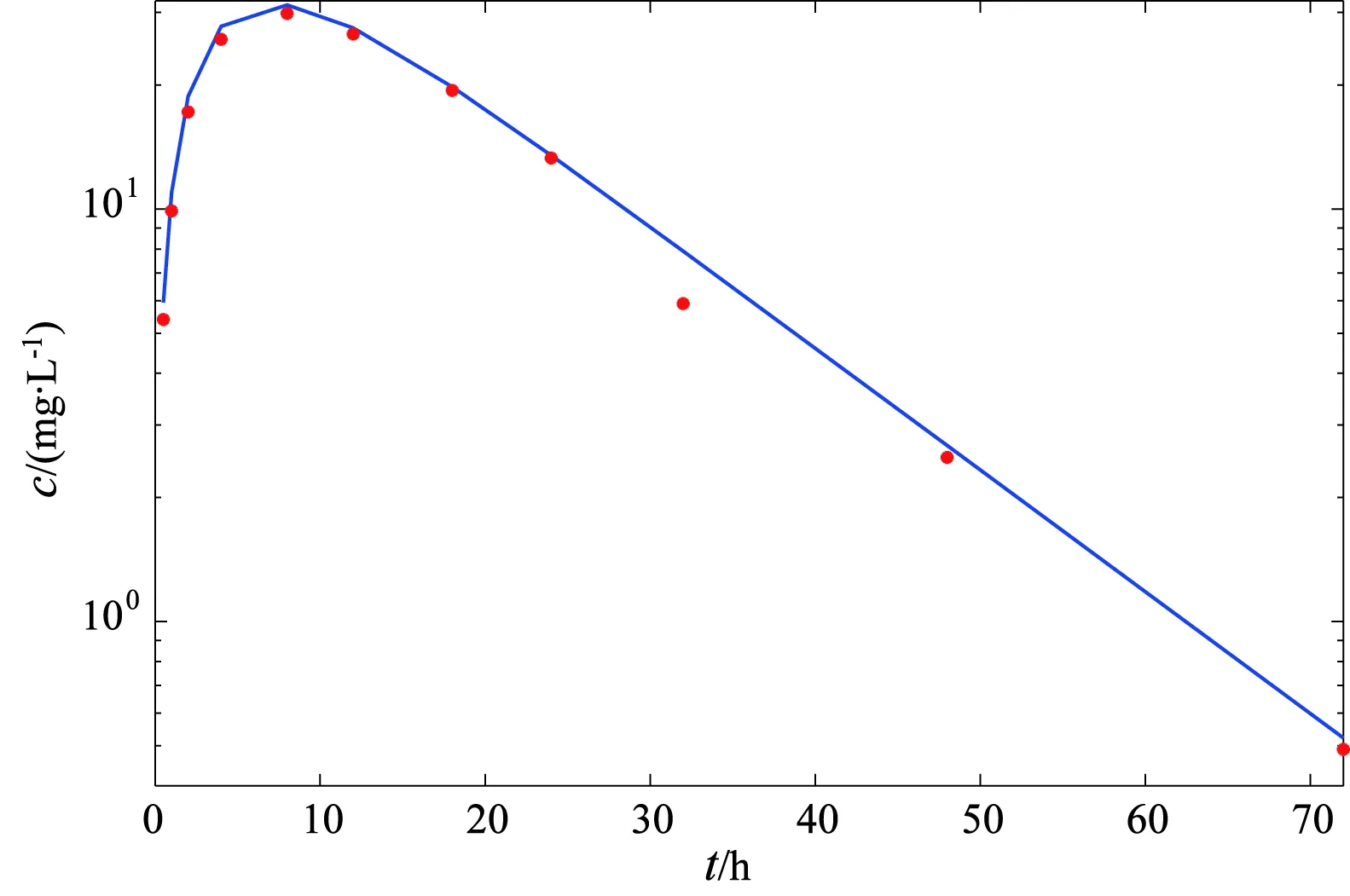
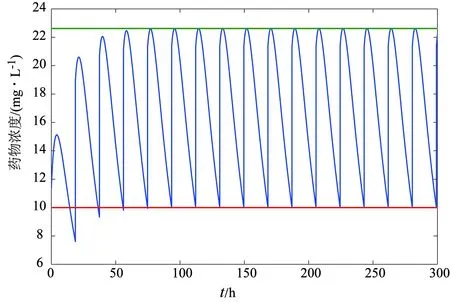
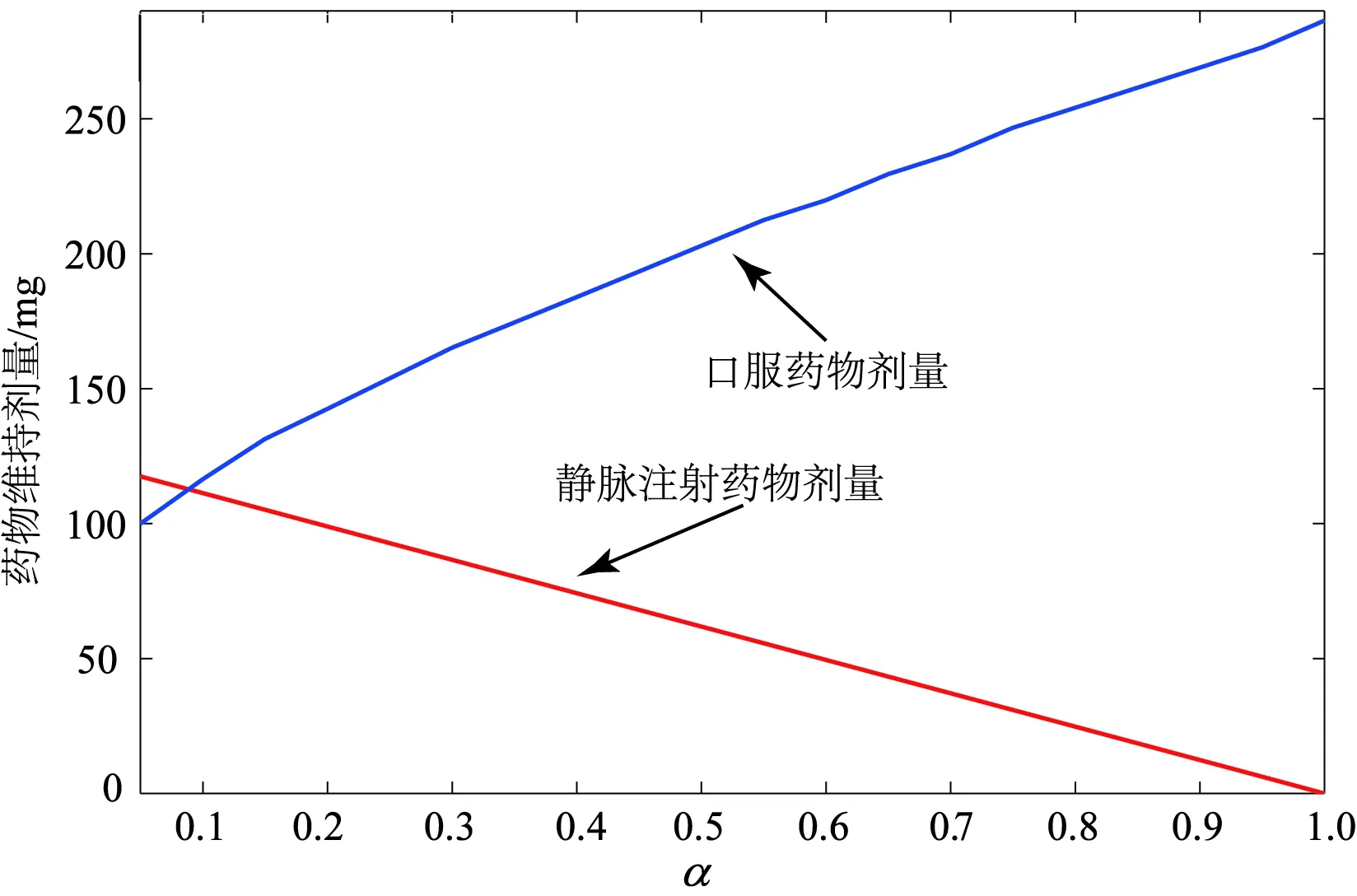
一般药物都有一个安全治疗窗口,指血药浓度所维持的有效范围,即介于最低有效浓度(MTL)和最低有毒浓度(MtoL)之间的区域。给药方案的设计是寻找合适的维持药量和给药的时间间隔使得MTL≤cmin ymax=vcmax,ymin=vcmin。 假定一级吸收率k0、一级消除率k1和表观分布容积v已知。从式(7)和式(8)易知,仅从固定ymax和ymin上确定静脉注射和口服给药的维持剂量及给药的时间间隔,则静脉注射联合口服给药方案是不唯一的。为了便于联合给药方案的设计,先固定y*的值,且使其满足y*∈(ymin,ymax),不妨令 y*=αymin+(1-α)ymax, 这里α∈(0,1),则可得静脉注射的维持剂量为 d1=y*-ymin=(1-α)(ymax-ymin)。 (9) 从式(9)可以看出,α的取值越大,需要的静脉注射的维持剂量d1的值越小,再由ymin的表达式(8),可得 (10) 由式(10)可以看出, 静脉注射的维持剂量d1的值越小,则需要口服药物的剂量d2的值就越大,也即是α的取值决定了静脉注射联合口服给药方案药物维持剂量的大小。α取值的多样性为在临床进行给药方案的设计带来很大的灵活性,可以结合不同患者的具体情况,进行个性化给药方案的设计。 通过式(9)可以求出静脉注射给药的剂量,但是式(7)和式(8)是关于口服药量d2和给药的时间间隔τ的非线性方程组,得到d2和τ的精确解存在困难。因此,可以借助计算机技术,采用一维搜索的计算方法, 得到合适的给药间隔τ,使得 |ymax-vMtoL|≤ε, 这里ε为控制精度所设置的一个非常小的正数。 为了保证口服剂量的值d2>0,则必然要求 ymin(1-e-k1τ)-d1e-k1τ>0 成立,也即是 (11) 这也就说明了τ的搜索起点应从τ*开始,进而最终确定一种可行的静脉注射联合口服给药方案。 由于y*的值选择具有多样性,这给临床上进行联合给药方案的设计带来更大的灵活性,有利于依据患者的实际情况制定更加合理的个性化给药方案。 依据理论分析和算法的设计原理,下面给出静脉注射联合口服给药方案的算法流程,并对具体的算例进行模拟仿真,进而给出具体的给药方案。 1)运用试验数据对药代动力学参数进行估计,也即是确定k0、k1和v。 2)选择合适的α值,可以先确定y*的值, y*=αymin+(1-α)ymax, 其中α∈(0,1),此时y*∈(ymin,ymax)。这里α的取值越大,口服给药的维持剂量越高,其值的选取要根据患者个体化的差异来进行设定。对于胃肠系统耐受较好的患者,α的取值可以稍大一些,而对于胃肠系统耐受较差的患者,α的取值可以稍小一些。 3) 由式(9)可得静脉注射给药剂量 d1=(1-α)(ymax-ymin)。 4)设定精度控制参数ε的值和搜索的步长h,其中步长越小精度越高,但是搜索的次数越多,具体一维搜索程序如下: 初始τ=τ*,将τ代入式(7)计算ymax的值; while abs(ymax-vMtoL)>ε τ=τ+h; 再次将τ代入式(7)计算ymax的值; end 返回的τ值即为给药的时间间隔。 5)将求得的给药时间间隔τ的值代入式(10)即可得到口服给药的剂量d2。 6)结合模型(1),运用Matlab中微分方程数值解的函数ode45,求出模型(1)的数值解,并给出药量随时间变化的图形。 利用文献[9]中的血药浓度时序数据来印证本文算法的合理性。假定口服某种溶液剂555.6 mg,定时取样,测得不同时间t的血药浓度c,如表1所示。 表1 血药浓度时序数据Tab. 1 Time series data of blood drug concentration 已知口服该药物的生物利用率f=0.9,最低有效浓度和最低有毒浓度分别为10.0 mg/L和22.6 mg/L,则可以给出具体的联合给药方案的设计流程。 血药浓度随时间变化的半对数图如图1所示。由图1可以看出,12 h以后的数据点基本在一条直线上。按照文献[8]中介绍的残数法来求该药物的动力学参数,可以得到药物的一级吸收率k0=0.252 h-1,一级消除率k1=0.068 h-1,患者的表观分布容积v=9.8 L。 图1 血药浓度时间序列半对数图形Fig. 1 Time series of semilog graph about blood drug concentration 为了验证算法的合理性和可行性,取α=0.1,则 y*=0.1ymin+0.9ymax=209.312 0。 由式(18)可得静脉注射的维持剂量为 d1=y*-ymin=209.312 0-98=111.312 0。 同样取ε=0.1,步长h=0.1,由式(11)可得τ*=11.20,对τ的搜索从11.2开始,步长h,直到 η=|ymax-vMtoL|= 为止,可得给药的时间间隔τ=18.70 h,将给药时间间隔τ的值代入到式(10)中可得口服给药的药量为d2=116.460 3,则稳态情况下患者体内药量的达峰时刻为 tmax=nτ+2.26, 一个给药时间间隔的平均稳态药量水平为 此时血药浓度的变化情况如图2所示。图2显示,经过3次口服给药后血药浓度趋于稳定,且稳态的血药浓度处于安全用药窗口之内。 可以发现,该联合给药方案采用静脉注射和口服给药的药量都是小剂量的给药方式,这与文献[2]中的静脉注射联合小剂量的口服给药方式是一致的。 为了进一步得到α的取值对给药方案设计影响,下面通过数值计算的方法给出静脉注射维持剂量、口服药物维持剂量和给药的时间间隔随α变化情况,分别见图3和图4。 图2 当d1=111.31,d2=116.40,τ=18.70时,联合给药下的血药浓度时间序列图Fig. 2 Time series of drug concentration under combined administration when d1=111.31,d2=116.40 and τ=18.70 图3 维持剂量随α的变化情况Fig. 3 The maintenance dose changes with respect to α 从图3可以看出,α的取值越大,口服给药的维持剂量越高,而静脉注射的维持剂量越小,这与前面的理论分析结果是一致的。从图4可以看出,随着α值的增加,给药的时间间隔也在增加。同时也表明,每给定一个α值,就可以得到一种可行的给药方案,对于不同的患者,应该结合患者的具体情况,选择合适的α值,为患者制定个体化的给药方案,以期取得最佳的治疗效果。 图4 给药时间间隔随α的变化情况Fig. 4 Dosing interval changes with respect to α 通过计算机辅助设计的方法,运用一房室模型研究了静脉注射联合口服给药方案的设计问题,首先从理论上导出了最小血药浓度和最大血药浓度的具体表达式和药物的达峰时间; 然后结合药物的安全窗口范围,详细地给出了静脉注射联合口服给药方案设计的算法原理和算法的具体流程;3.1 算法流程
3.2 算例分析


最后通过算例分析,验证了设计的算法的合理性和有效性。理论分析过程中发现,α的取值越大,口服给药的维持剂量就越高。因此,可以根据患者的实际情况选择合适的α值,具有针对性地设计个性化的治疗方案。比如,有些患者胃肠系统对口服药物的耐受是不相同的,对于肠胃功能差、对药物耐受较差的患者,可以采用小剂量口服给药方式,取小的α值;而对于肠胃功能好的、对药物耐受性较好的患者,可以采用大剂量的口服给药方式。因此,联合给药方式具有更多的灵活性,对患者进行临床个性化给药方案设计具有一定的参考价值。